LY4170156(Sofetabart Mipitecan)作为礼来公司打造的新一代FRα靶向ADC药物,之所以能在临床试验中展现出卓越的疗效与安全性,核心在于其精准的分子设计与革新性的作用机制。与同类FRα靶向ADC相比,LY4170156通过“Fc沉默抗体+专有可裂解连接子+强效载荷”的三位一体创新设计,实现了“靶向性更强、毒性更低、疗效更优”的突破,破解了传统ADC药物“脱靶毒性高、疗效局限、耐药风险高”的痛点,成为FRα靶向治疗领域的“最优解”之一。
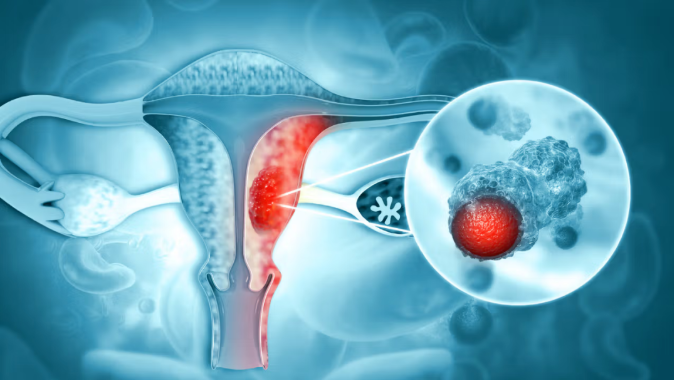
要理解LY4170156的作用机制,首先需明确FRα靶点的临床价值。FRα(叶酸受体α)是一种细胞表面糖蛋白,由FOLR1基因编码,其核心功能是结合叶酸并将其转运至细胞内,为细胞分裂和生长提供必需营养。在正常人体组织中,FRα仅在胎盘、肾脏等少数组织中低水平表达,而在卵巢癌、非小细胞肺癌、结直肠癌等多种实体瘤中过度表达,其中高级别浆液性卵巢癌的FRα阳性率高达90%,成为此类肿瘤精准治疗的理想靶点。传统FRα靶向ADC药物虽能针对该靶点发挥作用,但存在诸多设计缺陷,导致疗效与安全性难以平衡。
LY4170156的第一大核心创新,是采用Fc沉默的FRα特异性人源化单克隆抗体。与传统ADC的抗体不同,LY4170156的抗体经过L1-engineered Fc沉默修饰(LALA变体),可关闭FcγR结合能力,彻底阻断抗体依赖的细胞毒性(ADCC)和补体依赖的细胞毒性(CDC)。这种设计的优势在于,让抗体摆脱了“免疫杀伤”的额外功能,专注于“靶向运载”作用,既避免了ADCC/CDC带来的免疫相关毒性(如输液反应),又减少了抗体与正常组织的非特异性结合,大幅提升了靶向性,尤其适合FRα低表达的肿瘤患者,为后续全谱FRα表达患者的疗效覆盖奠定了基础。
第二大创新是采用礼来专有可裂解聚肌氨酸连接子(PSARlink™)。连接子是ADC药物的“灵魂”,其稳定性与裂解效率直接决定了药物的疗效与毒性。LY4170156的PSARlink™连接子具有两大核心优势:一是血浆稳定性极高,可在血液循环中保持稳定,避免连接子提前裂解导致载荷泄露,降低脱靶毒性;二是能在肿瘤细胞内的酸性环境或特定酶活性作用下快速裂解,裂解效率超过90%,可将载荷精准释放至肿瘤细胞内,最大化发挥杀伤作用。相比之下,同类药物的不可裂解连接子依赖溶酶体降解,不仅释放效率低,还易导致载荷在正常组织中泄露,引发眼部毒性等不良反应。
第三大创新是选用拓扑异构酶I抑制剂依沙替康(EXATECAN)作为载荷。依沙替康是一种强效拓扑异构酶I抑制剂,其作用机制是抑制肿瘤细胞DNA拓扑异构酶I的活性,阻止DNA复制与修复,从而诱导肿瘤细胞凋亡。与同类ADC常用的DM4微管抑制剂相比,依沙替康具有两大优势:一是抗肿瘤活性更强,且具有独特的旁观者效应,可杀死肿瘤细胞周围未表达FRα的肿瘤细胞,有效应对肿瘤异质性问题;二是毒性谱更可控,不易引发眼部毒性和周围神经病变,与连接子的设计形成协同,进一步提升了药物的安全性。此外,LY4170156的药物抗体比(DAR)为8,可确保每个抗体分子携带足够的载荷,实现“精准给药、强效杀伤”的双重目标。
(责任编辑:香港祺昌医药公司)
